MCTel2
Zitat von Martin Kneppeck am 2. November 2025, 16:56 UhrBesuchsgrund einer Neukundin: Optometrische Untersuchung der Augen, Optimierung des Sehens; Gefühl zu Schielen
Allgemein: 2014 und 2017 Diagnose Brustkrebs mit Behandlung; Kolitis
Augen:
Bergmann Augenklinik 16.05.2022:
RA: + 0,75 – 3,00 172° Vcc 0,8 LA: + 0,25 -2,25 13° Vcc 0,5
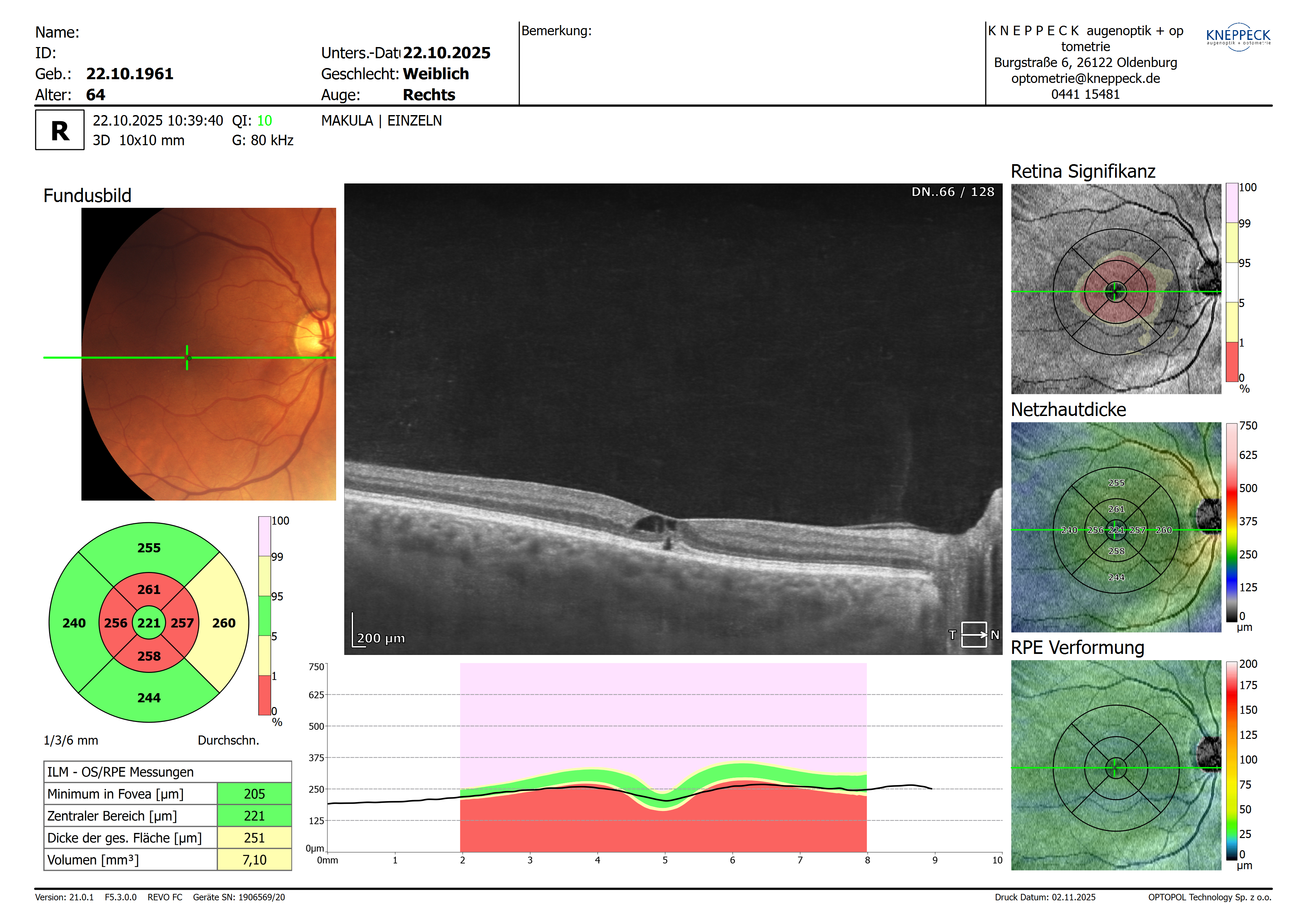
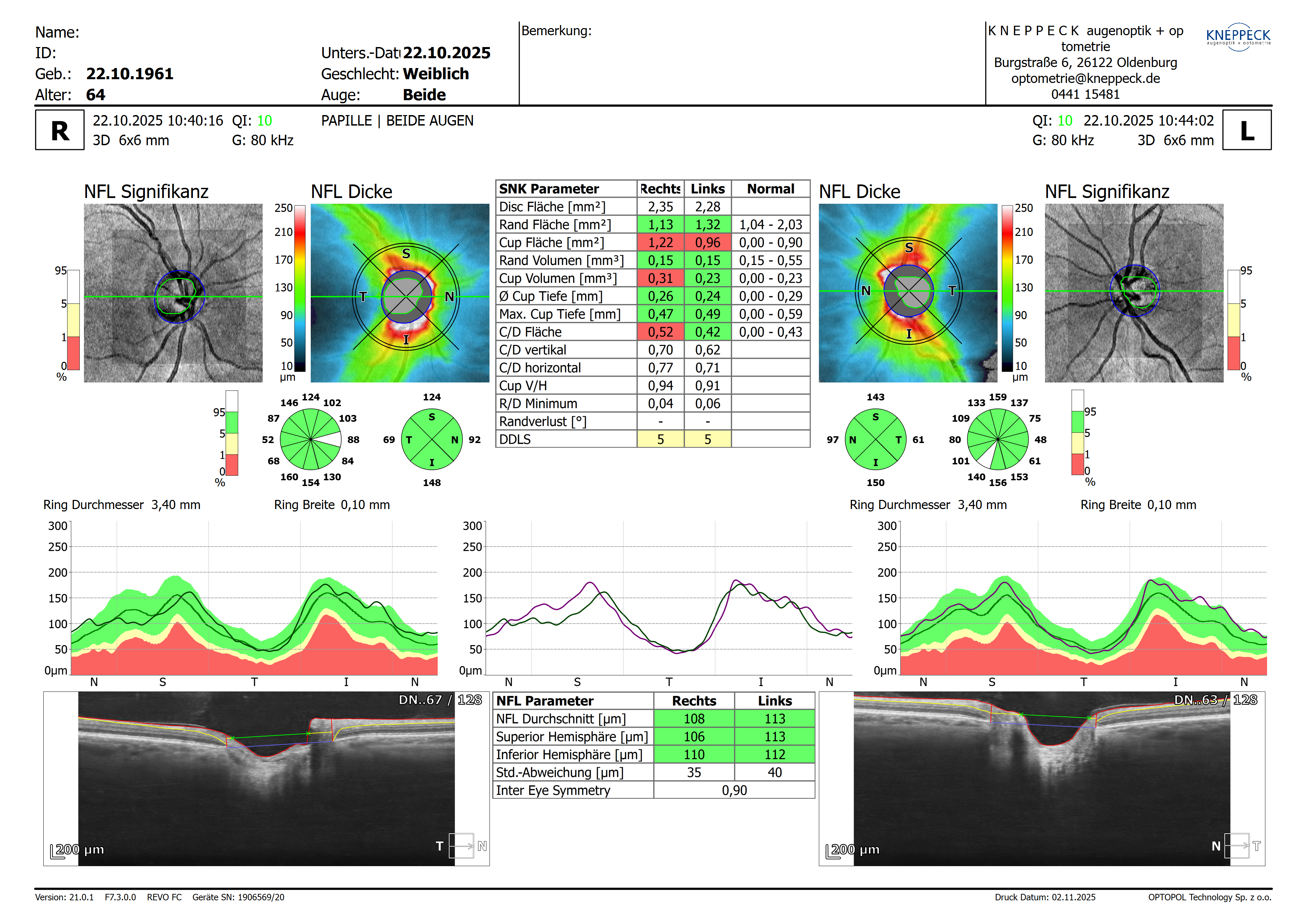
Diagnose MCTel2; CDR rechts: 0,4 CDR links: 0,6 „In der OCT-Untersuchung zeigen sich bds. Pseudo-zystische Auflockerungen der inneren retinalen Nervenfaserschichten. Ferner zeigte sich beim LA zusätzlich eine leichte Auflockerung der ellipsoiden Zone. In der ergänzenden Fluoreszenzangiographie sahen wir bds. eine frühe deutliche Leckage“.
Bergmann Augenklinik 02.06.2024:
RA: + 1,00 – 3,25 174° Vcc 0,8 LA: + 0,50 -2,00 17° Vcc 0,8
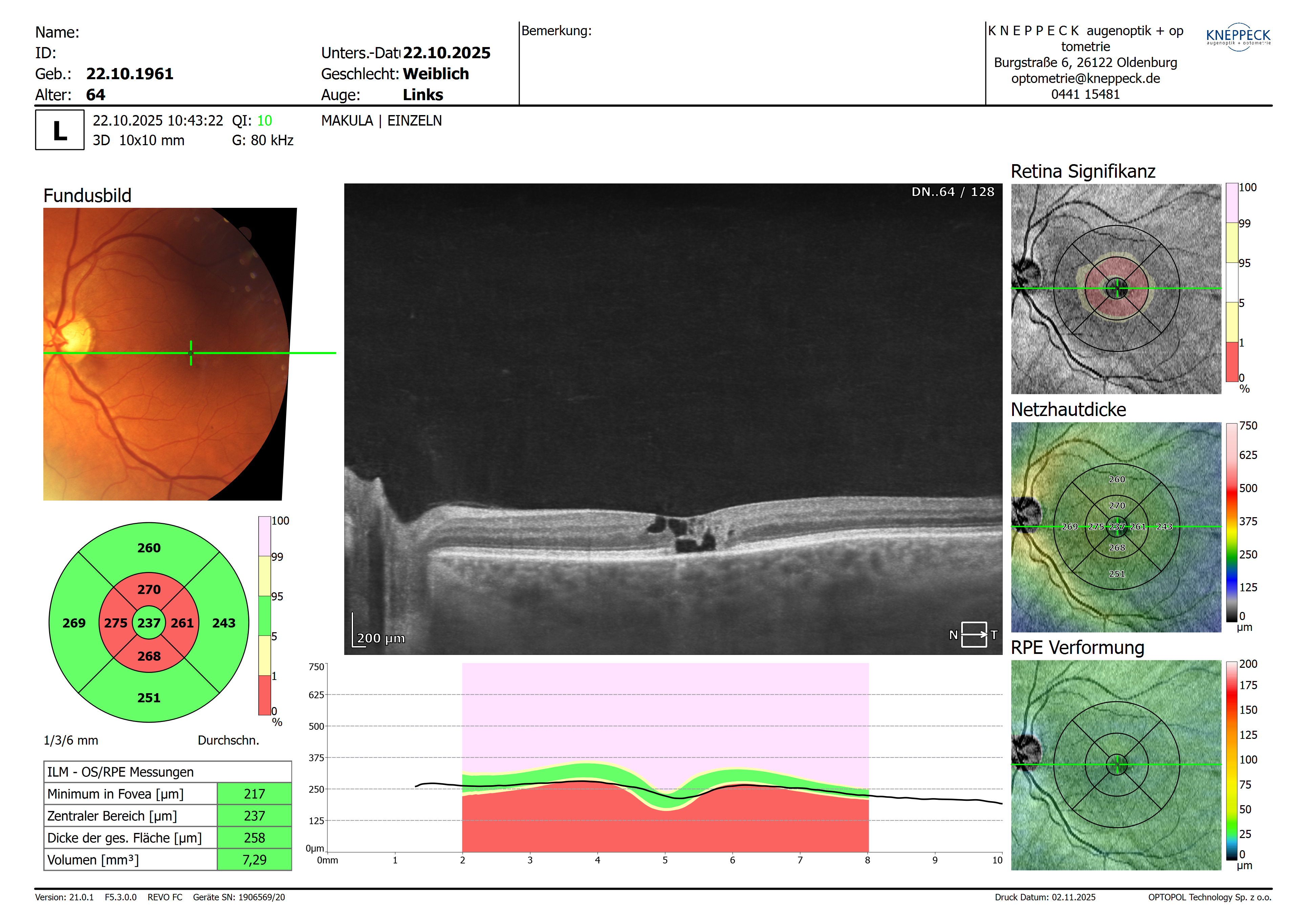
CDR rechts: 0,6-0,7 „Makula: aufgelockert, Verbeiterung der fovealen Senke, keine frische Blutung, NH anliegend“ CDR links: 0,5 „Makula: aufgelockert, fleckförmiges Aussehen der Fovea, keine frische Blutung, NH anliegend…. In der optischen Kohärenztomographie imponieren an beiden Augen die vorbeschriebenen intraretinalen Kavernen mit Gewebebrücken ohne Anhalt für eine Progression im OCT-Vergleich….“
Meine Messungen 22.10.2025:
RA: +1,12 -3,75 177° Vcc 0,4 LA: 0,37 -2,00 18° Vcc 0,50
Vorderer Augenabschnitt: HH befundfrei; geringe Tränenfilmmenge mit kurzer Aufreißzeit; dadurch bedingt instabiler Visus
NCT 10:23 h: RA: IODc: 21,9 mm/Hg LA: IODc: 21,5 mm/Hg
RA: Kammerwinkel N:23° T:24° LA: Kammerwinkel N:23° T:23°
Beide Augenlinsen zeigen im Kern punktuelle Trübungsstellen (beim rechten Auge ausgeprägter). Diese befinden sich außerhalb der optischen Achse und sind nicht visusrelevant.
Gesichtsfeld: Bei beiden Augen zentrale Gesichtsfeldausfälle. In der Optotypenreihe werden bei beiden Augen Sehzeichen nicht gesehen. Diese können nur durch Blickbewegungen gefunden werden. Die Geschichtsfeldmessung mit dem FDT-Perimeter ist fast vollständig unauffällig.
- Ist für diese Diskrepanz der zu große Abstand der Messpunkte verantwortlich (fallen kleinere Defekte durch das Raster)?
- FAF RA: in der INL erweiterte Kapillare temporal der Fovea > Das kann ich mir erklären. FAF LA: in der INL ist das Kapillarnetz inferior der Fovea reduziert > Habt ihr eine Erklärung dafür?
- Ist die kreisförmige Atrophie um Fovea typisch für MCTel2?
- Gibt es (auch off-label) eine Therapiemöglichkeit?
Vielen Dank im Voraus für Eure Unterstützung!
Besuchsgrund einer Neukundin: Optometrische Untersuchung der Augen, Optimierung des Sehens; Gefühl zu Schielen
Allgemein: 2014 und 2017 Diagnose Brustkrebs mit Behandlung; Kolitis
Augen:
Bergmann Augenklinik 16.05.2022:
RA: + 0,75 – 3,00 172° Vcc 0,8 LA: + 0,25 -2,25 13° Vcc 0,5
Diagnose MCTel2; CDR rechts: 0,4 CDR links: 0,6 „In der OCT-Untersuchung zeigen sich bds. Pseudo-zystische Auflockerungen der inneren retinalen Nervenfaserschichten. Ferner zeigte sich beim LA zusätzlich eine leichte Auflockerung der ellipsoiden Zone. In der ergänzenden Fluoreszenzangiographie sahen wir bds. eine frühe deutliche Leckage“.
Bergmann Augenklinik 02.06.2024:
RA: + 1,00 – 3,25 174° Vcc 0,8 LA: + 0,50 -2,00 17° Vcc 0,8
CDR rechts: 0,6-0,7 „Makula: aufgelockert, Verbeiterung der fovealen Senke, keine frische Blutung, NH anliegend“ CDR links: 0,5 „Makula: aufgelockert, fleckförmiges Aussehen der Fovea, keine frische Blutung, NH anliegend…. In der optischen Kohärenztomographie imponieren an beiden Augen die vorbeschriebenen intraretinalen Kavernen mit Gewebebrücken ohne Anhalt für eine Progression im OCT-Vergleich….“
Meine Messungen 22.10.2025:
RA: +1,12 -3,75 177° Vcc 0,4 LA: 0,37 -2,00 18° Vcc 0,50
Vorderer Augenabschnitt: HH befundfrei; geringe Tränenfilmmenge mit kurzer Aufreißzeit; dadurch bedingt instabiler Visus
NCT 10:23 h: RA: IODc: 21,9 mm/Hg LA: IODc: 21,5 mm/Hg
RA: Kammerwinkel N:23° T:24° LA: Kammerwinkel N:23° T:23°
Beide Augenlinsen zeigen im Kern punktuelle Trübungsstellen (beim rechten Auge ausgeprägter). Diese befinden sich außerhalb der optischen Achse und sind nicht visusrelevant.
Gesichtsfeld: Bei beiden Augen zentrale Gesichtsfeldausfälle. In der Optotypenreihe werden bei beiden Augen Sehzeichen nicht gesehen. Diese können nur durch Blickbewegungen gefunden werden. Die Geschichtsfeldmessung mit dem FDT-Perimeter ist fast vollständig unauffällig.
- Ist für diese Diskrepanz der zu große Abstand der Messpunkte verantwortlich (fallen kleinere Defekte durch das Raster)?
- FAF RA: in der INL erweiterte Kapillare temporal der Fovea > Das kann ich mir erklären. FAF LA: in der INL ist das Kapillarnetz inferior der Fovea reduziert > Habt ihr eine Erklärung dafür?
- Ist die kreisförmige Atrophie um Fovea typisch für MCTel2?
- Gibt es (auch off-label) eine Therapiemöglichkeit?
Vielen Dank im Voraus für Eure Unterstützung!
Hochgeladene Dateien:
Zitat von Joshua Torrent Despouy am 3. November 2025, 00:03 UhrHallo liebes Forum,
das ist ein wirklich faszinierender Fall!
Zunächst einmal vielen herzlichen Dank für die ausführliche Vorstellung und die beeindruckenden Bildaufnahmen – sowohl die OCTs als auch die OCT-Angiografien sind hervorragend und zeigen das Krankheitsbild in bemerkenswerter Klarheit.Bei den Visuserhebungen fällt auf, dass die Werte im Verlauf gewisse Schwankungen zeigen. Diese sind einerseits mit einer instabilen Tränenfilmqualität vereinbar, können aber auch durch den in der OCT sichtbaren zentralen Defekt und das daraus resultierende zentrale Skotom erklärt werden.
Da der Defekt sehr klein ist, handelt es sich funktionell um ein Mikroskotom. Das Gehirn kompensiert diesen kleinen Ausfall durch exzentrische Fixation, sodass die Patientin im Alltag kaum Einschränkungen bemerkt. Der subjektive Leidensdruck bleibt daher meist gering.
Die durchgeführte Perimetrie ist für die Darstellung solcher kleinen zentralen Defekte zu grob. Um diese präzise zu erfassen, eignet sich die Mikroperimetrie, die eine fein aufgelöste Sensitivitätskarte der Fovea liefert – ein Verfahren, das allerdings nur in spezialisierten Zentren verfügbar ist.
Die morphologischen Veränderungen passen sehr gut zum Bild einer makulären Teleangiektasie Typ 2.
Typischerweise ist diese Erkrankung beidseitig und zeigt im OCT die charakteristischen parafovealen, „mottenfraßähnlichen“ Zysten.Im Verlauf kommt es häufig zu einer Degeneration der äußeren Netzhautschichten – insbesondere der Photorezeptoren und des retinalen Pigmentepithels (RPE). Ein weiteres typisches Merkmal ist die Migration von RPE-Zellen in höhere Netzhautschichten, was auch in diesem Fall eindrücklich sichtbar ist.
Diese degenerativen Veränderungen können schließlich in eine foveale Atrophie übergehen.
Die MakTel Typ 2 unterscheidet sich deutlich von den meisten anderen Netzhauterkrankungen, da sie nicht primär vaskulär, sondern neurodegenerativ bedingt ist.
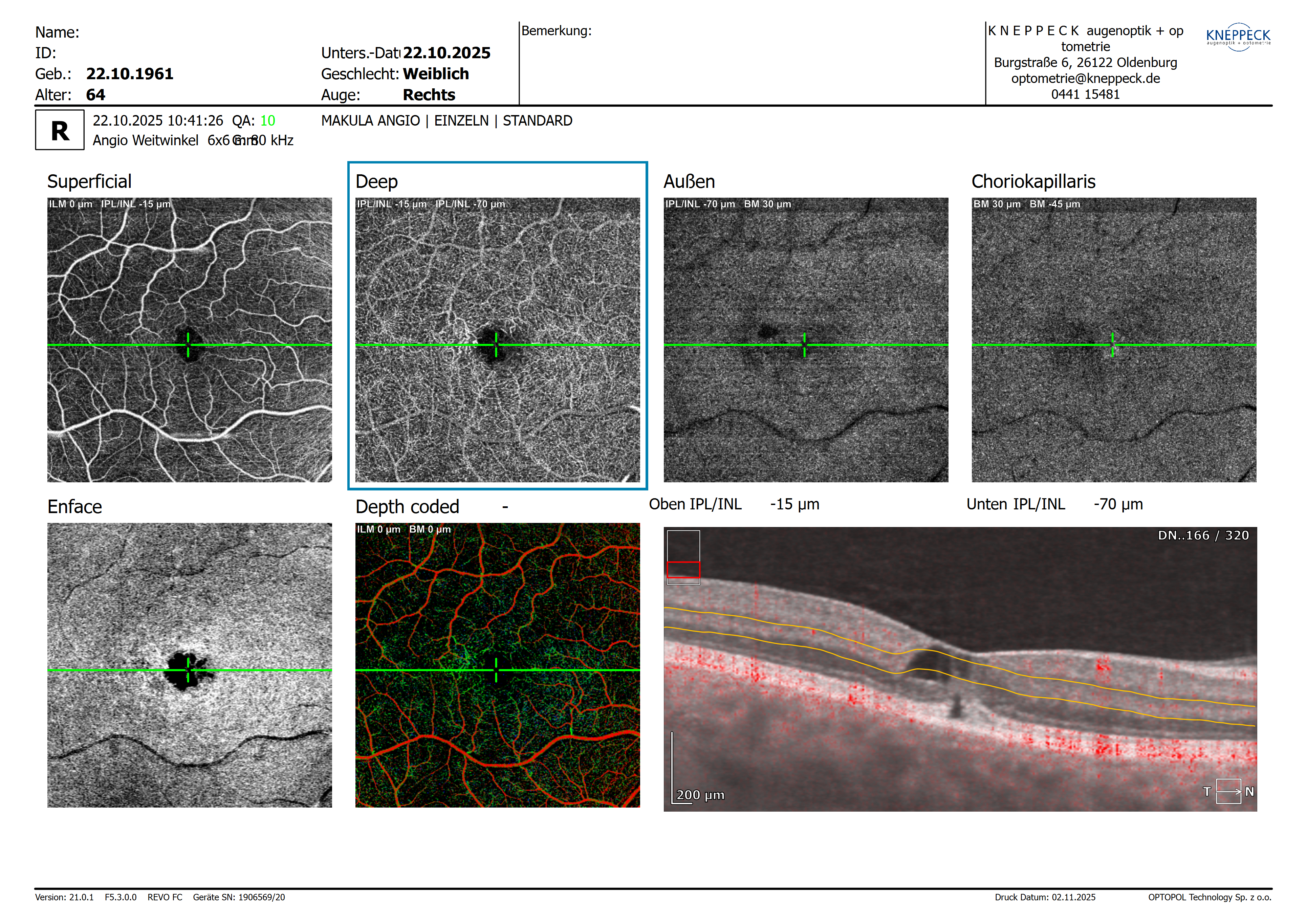
Zentral in der Pathogenese steht der Untergang der Müller’schen Stützzellen, die eine Schlüsselrolle für die strukturelle Integrität und metabolische Stabilität der Netzhaut spielen. Ihr Verlust führt zu sekundären Veränderungen in den Gefäßplexus, Photorezeptoren und im RPE.Die OCT-Angiografie-Aufnahmen sind besonders eindrucksvoll und zeigen klassische Merkmale der MacTel Typ 2:
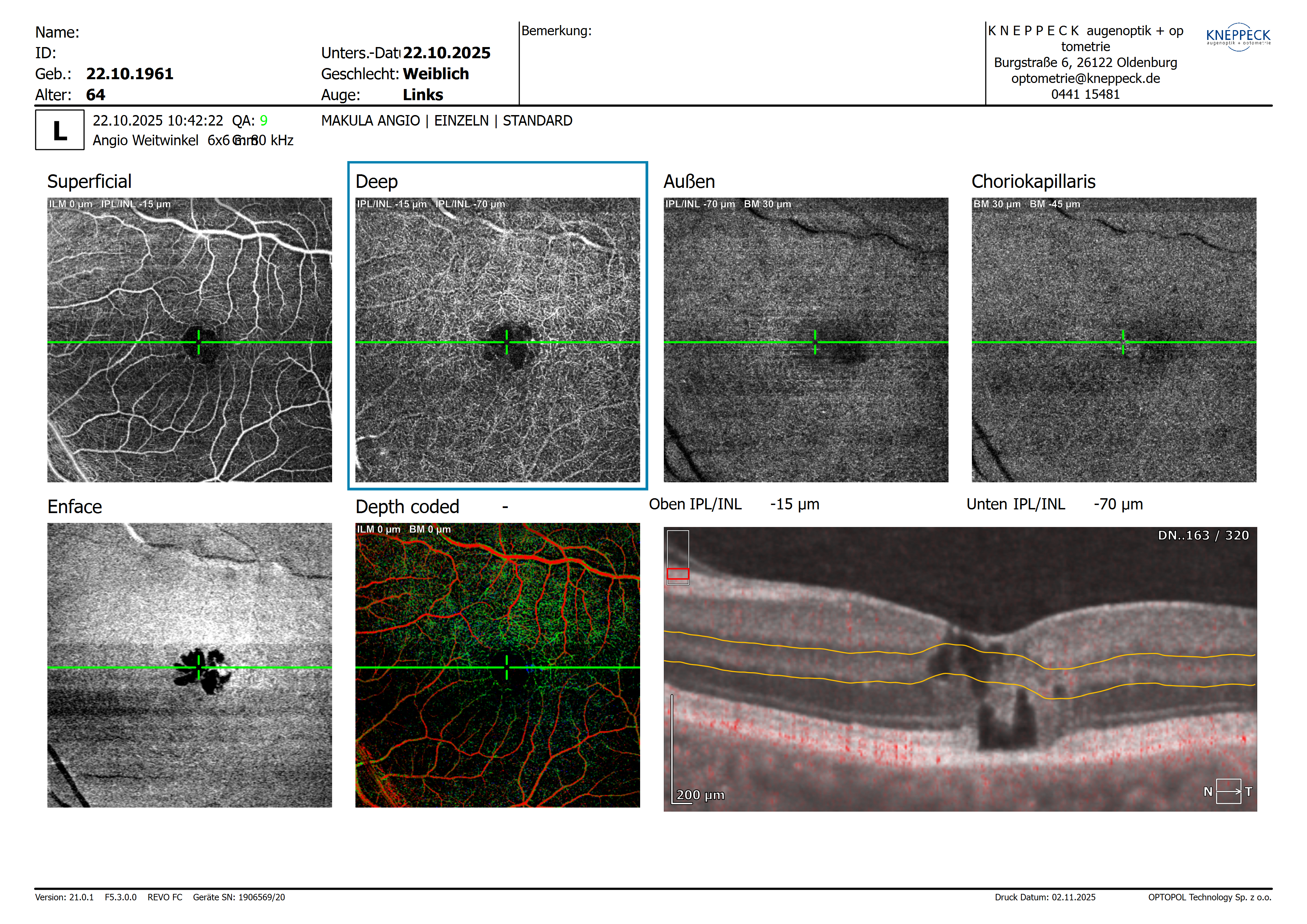
Verlust der kapillaren Dichte im tiefen Gefäßplexus,
Irreguläre, teils dilatierte Gefäßstrukturen im parafovealen Bereich,
und in der kolorierten Darstellung eine auffällige Irregularität des tiefen Plexus – ein typisches OCTA-Muster dieser Erkrankung.
Therapie:
Der Verlauf der MacTel Typ 2 ist in der Regel langsam progredient.
Die Sehschärfeverschlechterung schreitet, wenn überhaupt, über viele Jahre voran.Aktuell existiert keine etablierte Therapie, die den Krankheitsprozess aufhalten oder rückgängig machen kann.
Eine IVOM-Therapie mit Anti-VEGF ist nur bei sekundärer choroidaler Neovaskularisation (ca. 10–15 % der Fälle) indiziert. In allen anderen Stadien bleibt sie wirkungslos, da keine vaskuläre Komponente vorliegt.Ein vielversprechender neuer Ansatz ist das CNTF-Implantat (Ciliary Neurotrophic Factor).
Dieser neurotrophe Faktor soll Photorezeptoren und Müller-Zellen schützen und damit den degenerativen Prozess verlangsamen oder stabilisieren.
Erste klinische Studien zeigen eine potenzielle Wirksamkeit gegenüber Placebo.
Die intraokulären Implantate werden über eine IVOM-artige Technik appliziert und befinden sich derzeit sowohl in den USA als auch in Europa in fortgeschrittener klinischer Prüfung, sind aber noch nicht zugelassen.
Der Fall zeigt eindrucksvoll, wie degenerative Prozesse der Müller-Zellen komplexe strukturelle und funktionelle Veränderungen der Makula hervorrufen können – und wie wichtig die genaue Bildinterpretation für die korrekte Diagnose ist.Vielen Dank nochmals für die großartigen Aufnahmen und die eindrucksvolle Fallvorstellung!
Viele Grüße,
Dr. Joshua Torrent D.
Hallo liebes Forum,
das ist ein wirklich faszinierender Fall!
Zunächst einmal vielen herzlichen Dank für die ausführliche Vorstellung und die beeindruckenden Bildaufnahmen – sowohl die OCTs als auch die OCT-Angiografien sind hervorragend und zeigen das Krankheitsbild in bemerkenswerter Klarheit.
Bei den Visuserhebungen fällt auf, dass die Werte im Verlauf gewisse Schwankungen zeigen. Diese sind einerseits mit einer instabilen Tränenfilmqualität vereinbar, können aber auch durch den in der OCT sichtbaren zentralen Defekt und das daraus resultierende zentrale Skotom erklärt werden.
Da der Defekt sehr klein ist, handelt es sich funktionell um ein Mikroskotom. Das Gehirn kompensiert diesen kleinen Ausfall durch exzentrische Fixation, sodass die Patientin im Alltag kaum Einschränkungen bemerkt. Der subjektive Leidensdruck bleibt daher meist gering.
Die durchgeführte Perimetrie ist für die Darstellung solcher kleinen zentralen Defekte zu grob. Um diese präzise zu erfassen, eignet sich die Mikroperimetrie, die eine fein aufgelöste Sensitivitätskarte der Fovea liefert – ein Verfahren, das allerdings nur in spezialisierten Zentren verfügbar ist.
Die morphologischen Veränderungen passen sehr gut zum Bild einer makulären Teleangiektasie Typ 2.
Typischerweise ist diese Erkrankung beidseitig und zeigt im OCT die charakteristischen parafovealen, „mottenfraßähnlichen“ Zysten.
Im Verlauf kommt es häufig zu einer Degeneration der äußeren Netzhautschichten – insbesondere der Photorezeptoren und des retinalen Pigmentepithels (RPE). Ein weiteres typisches Merkmal ist die Migration von RPE-Zellen in höhere Netzhautschichten, was auch in diesem Fall eindrücklich sichtbar ist.
Diese degenerativen Veränderungen können schließlich in eine foveale Atrophie übergehen.
Die MakTel Typ 2 unterscheidet sich deutlich von den meisten anderen Netzhauterkrankungen, da sie nicht primär vaskulär, sondern neurodegenerativ bedingt ist.
Zentral in der Pathogenese steht der Untergang der Müller’schen Stützzellen, die eine Schlüsselrolle für die strukturelle Integrität und metabolische Stabilität der Netzhaut spielen. Ihr Verlust führt zu sekundären Veränderungen in den Gefäßplexus, Photorezeptoren und im RPE.
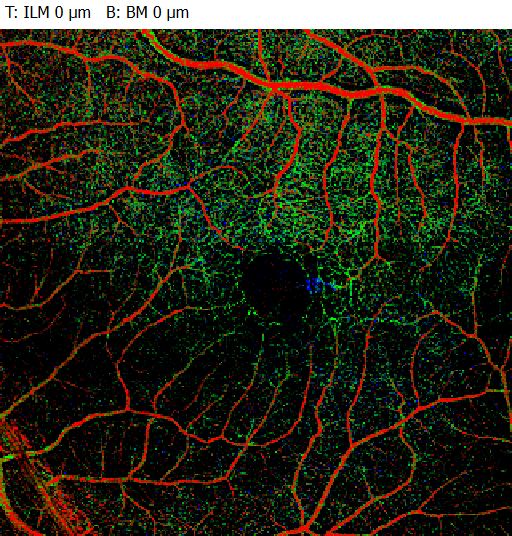
Die OCT-Angiografie-Aufnahmen sind besonders eindrucksvoll und zeigen klassische Merkmale der MacTel Typ 2:
-
Verlust der kapillaren Dichte im tiefen Gefäßplexus,
-
Irreguläre, teils dilatierte Gefäßstrukturen im parafovealen Bereich,
-
und in der kolorierten Darstellung eine auffällige Irregularität des tiefen Plexus – ein typisches OCTA-Muster dieser Erkrankung.
Therapie:
Der Verlauf der MacTel Typ 2 ist in der Regel langsam progredient.
Die Sehschärfeverschlechterung schreitet, wenn überhaupt, über viele Jahre voran.
Aktuell existiert keine etablierte Therapie, die den Krankheitsprozess aufhalten oder rückgängig machen kann.
Eine IVOM-Therapie mit Anti-VEGF ist nur bei sekundärer choroidaler Neovaskularisation (ca. 10–15 % der Fälle) indiziert. In allen anderen Stadien bleibt sie wirkungslos, da keine vaskuläre Komponente vorliegt.
Ein vielversprechender neuer Ansatz ist das CNTF-Implantat (Ciliary Neurotrophic Factor).
Dieser neurotrophe Faktor soll Photorezeptoren und Müller-Zellen schützen und damit den degenerativen Prozess verlangsamen oder stabilisieren.
Erste klinische Studien zeigen eine potenzielle Wirksamkeit gegenüber Placebo.
Die intraokulären Implantate werden über eine IVOM-artige Technik appliziert und befinden sich derzeit sowohl in den USA als auch in Europa in fortgeschrittener klinischer Prüfung, sind aber noch nicht zugelassen.
Der Fall zeigt eindrucksvoll, wie degenerative Prozesse der Müller-Zellen komplexe strukturelle und funktionelle Veränderungen der Makula hervorrufen können – und wie wichtig die genaue Bildinterpretation für die korrekte Diagnose ist.
Vielen Dank nochmals für die großartigen Aufnahmen und die eindrucksvolle Fallvorstellung!
Viele Grüße,
Dr. Joshua Torrent D.
Zitat von Martin Kneppeck am 3. November 2025, 12:17 UhrVielen Dank für ihre ausführliche Antwort Herr Dr. Torrent Despouy!
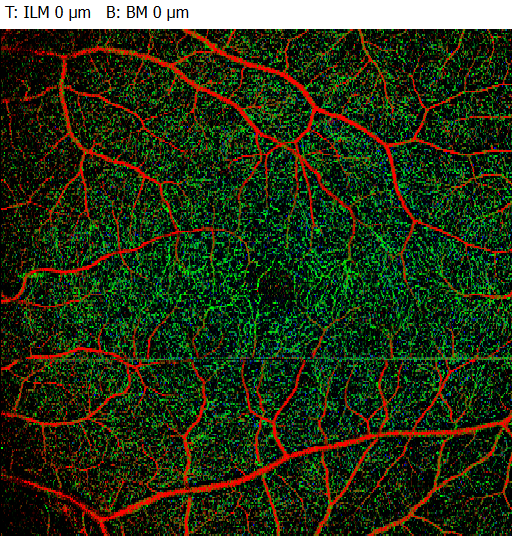
Könnten Sie mir den Grund für den Verlust der kapillaren Dichte im tiefen Gefäßplexus beim linken Auge (grün codiert) nennen? Was bewirkt der Untergang der Müller’schen Stützzellen? Kollabieren dann die Gefäßwände aufgrund des Perizytenverlustes? Zum Bild-Vergleich habe ich die Darstellung eines gesunden Auges eingefügt.
An wen könnte meine Kundin sich wenden um sich für eine Studie des in der Testphase befindlichen CNTF-Implantat zu bewerben?
Mir ist bewusst, dass Sie stark ausgelastet sind – vielen Dank für daher nochmals für ihre ausführlichen und differenzierten Antworten (ich habe bisher jede gelesen)!
Herzliche Grüße, Martin Kneppeck
PS: Bei meiner Frage 2 hatte ich versehentlich in Folge von copy and paste FAF anstelle OCT-A eingefügt. Ich bitte dies gedanklich auszutauschen 😉
Vielen Dank für ihre ausführliche Antwort Herr Dr. Torrent Despouy!
Könnten Sie mir den Grund für den Verlust der kapillaren Dichte im tiefen Gefäßplexus beim linken Auge (grün codiert) nennen? Was bewirkt der Untergang der Müller’schen Stützzellen? Kollabieren dann die Gefäßwände aufgrund des Perizytenverlustes? Zum Bild-Vergleich habe ich die Darstellung eines gesunden Auges eingefügt.
An wen könnte meine Kundin sich wenden um sich für eine Studie des in der Testphase befindlichen CNTF-Implantat zu bewerben?
Mir ist bewusst, dass Sie stark ausgelastet sind – vielen Dank für daher nochmals für ihre ausführlichen und differenzierten Antworten (ich habe bisher jede gelesen)!
Herzliche Grüße, Martin Kneppeck
PS: Bei meiner Frage 2 hatte ich versehentlich in Folge von copy and paste FAF anstelle OCT-A eingefügt. Ich bitte dies gedanklich auszutauschen 😉
Hochgeladene Dateien:Zitat von Joshua Torrent Despouy am 3. November 2025, 23:16 UhrHallo Herr Kneppeck,
für das Forum nehme ich mir immer gerne Zeit – der fachliche Austausch hier ist nicht nur bereichernd, sondern auch etwas, das ich mit Leidenschaft unterstütze. Es ist schön zu sehen, wie engagiert und tiefgehend hier diskutiert wird!
Ihr Fall zeigt auf eindrucksvolle Weise, welch zentrale Rolle die Müller’schen Stützzellen in der Netzhaut einnehmen.
Meiner Meinung nach sind sie eine der am meisten unterschätzten Zellpopulationen der Retina – und doch bilden sie das funktionelle Rückgrat des retinalen Gewebes. Ich habe einmal einen ganzen Vortrag ausschließlich diesen Zellen gewidmet – und das zurecht: Sie sind die „stillen Helden“ unserer Netzhaut!Leider führt gerade diese enorme funktionelle Bedeutung dazu, dass jede Störung oder Degeneration der Müller’schen Zellen weitreichende Folgen für die Netzhautarchitektur und -funktion hat.
In Ihrem Bildvergleich erkennt man sehr schön die typischen Veränderungen des Kapillarplexus im Vergleich zu einer gesunden Netzhaut. Besonders betroffen ist hier der tiefe kapilläre Plexus (Deep Capillary Plexus, DCP).
Anatomisch liegt dieser Plexus in unmittelbarer Nähe zu den Endfüßen der Müller-Zellen und den Photorezeptoren – eine enge funktionelle und metabolische Verbindung, die seine besondere Vulnerabilität erklärt. Die Degeneration oder Dysfunktion der Müller-Zellen wirkt sich daher unmittelbar auf die Stabilität und Integrität dieser Gefäßschicht aus.
Die Schädigung der tiefen Kapillaren beruht auf mehreren pathophysiologischen Prozessen:
Verlust trophischer Unterstützung:
Müller-Zellen stabilisieren die Kapillarwände, regulieren den Blutfluss und schützen Endothelzellen vor oxidativem Stress. Fällt diese Unterstützung weg, kommt es zu struktureller Instabilität, Gefäßwandveränderungen und letztlich zur Kapillarregression.Leckage und Ödembildung:
Die Degeneration der Zellfortsätze, die eng mit den Kapillaren des DCP verbunden sind, führt zu Permeabilitätsstörungen der Gefäßwände. Flüssigkeit tritt in die Netzhaut ein – im OCT zeigt sich dies als intra- oder subretinales Ödem.Lokale Hypoxie und metabolische Dysregulation:
Der gestörte Austausch zwischen Müller-Zellen, Photorezeptoren und Kapillaren führt zu Sauerstoffmangel und energetischem Ungleichgewicht, insbesondere im Bereich der Photorezeptoren und des RPE.
Langfristig entstehen degenerative Umbauprozesse bis hin zur lokalen Atrophie.Bezüglich möglicher Therapieoptionen liegen derzeit in Deutschland nur wenige klinische Erfahrungen vor.
Nach meinem Kenntnisstand ist aktuell noch unklar, welche deutschen Zentren an den laufenden Zulassungsstudien beteiligt sind. Die bisherigen Erkenntnisse stammen überwiegend aus der Literatur.Ich werde mich hierzu gerne noch genauer informieren – die Forschung in diesem Bereich ist ausgesprochen spannend und entwickelt sich dynamisch.
Vielen Dank für die wertvolle Diskussion und die großartigen Bildbeispiele!
Ich wünsche allen einen schönen Abend und danke herzlich für die wertschätzenden Worte.
Viele Grüße,
Dr. med. Joshua Torrent D.
Hallo Herr Kneppeck,
für das Forum nehme ich mir immer gerne Zeit – der fachliche Austausch hier ist nicht nur bereichernd, sondern auch etwas, das ich mit Leidenschaft unterstütze. Es ist schön zu sehen, wie engagiert und tiefgehend hier diskutiert wird!
Ihr Fall zeigt auf eindrucksvolle Weise, welch zentrale Rolle die Müller’schen Stützzellen in der Netzhaut einnehmen.
Meiner Meinung nach sind sie eine der am meisten unterschätzten Zellpopulationen der Retina – und doch bilden sie das funktionelle Rückgrat des retinalen Gewebes. Ich habe einmal einen ganzen Vortrag ausschließlich diesen Zellen gewidmet – und das zurecht: Sie sind die „stillen Helden“ unserer Netzhaut!
Leider führt gerade diese enorme funktionelle Bedeutung dazu, dass jede Störung oder Degeneration der Müller’schen Zellen weitreichende Folgen für die Netzhautarchitektur und -funktion hat.
In Ihrem Bildvergleich erkennt man sehr schön die typischen Veränderungen des Kapillarplexus im Vergleich zu einer gesunden Netzhaut. Besonders betroffen ist hier der tiefe kapilläre Plexus (Deep Capillary Plexus, DCP).
Anatomisch liegt dieser Plexus in unmittelbarer Nähe zu den Endfüßen der Müller-Zellen und den Photorezeptoren – eine enge funktionelle und metabolische Verbindung, die seine besondere Vulnerabilität erklärt. Die Degeneration oder Dysfunktion der Müller-Zellen wirkt sich daher unmittelbar auf die Stabilität und Integrität dieser Gefäßschicht aus.
Die Schädigung der tiefen Kapillaren beruht auf mehreren pathophysiologischen Prozessen:
-
Verlust trophischer Unterstützung:
Müller-Zellen stabilisieren die Kapillarwände, regulieren den Blutfluss und schützen Endothelzellen vor oxidativem Stress. Fällt diese Unterstützung weg, kommt es zu struktureller Instabilität, Gefäßwandveränderungen und letztlich zur Kapillarregression. -
Leckage und Ödembildung:
Die Degeneration der Zellfortsätze, die eng mit den Kapillaren des DCP verbunden sind, führt zu Permeabilitätsstörungen der Gefäßwände. Flüssigkeit tritt in die Netzhaut ein – im OCT zeigt sich dies als intra- oder subretinales Ödem. -
Lokale Hypoxie und metabolische Dysregulation:
Der gestörte Austausch zwischen Müller-Zellen, Photorezeptoren und Kapillaren führt zu Sauerstoffmangel und energetischem Ungleichgewicht, insbesondere im Bereich der Photorezeptoren und des RPE.
Langfristig entstehen degenerative Umbauprozesse bis hin zur lokalen Atrophie.
Bezüglich möglicher Therapieoptionen liegen derzeit in Deutschland nur wenige klinische Erfahrungen vor.
Nach meinem Kenntnisstand ist aktuell noch unklar, welche deutschen Zentren an den laufenden Zulassungsstudien beteiligt sind. Die bisherigen Erkenntnisse stammen überwiegend aus der Literatur.
Ich werde mich hierzu gerne noch genauer informieren – die Forschung in diesem Bereich ist ausgesprochen spannend und entwickelt sich dynamisch.
Vielen Dank für die wertvolle Diskussion und die großartigen Bildbeispiele!
Ich wünsche allen einen schönen Abend und danke herzlich für die wertschätzenden Worte.
Viele Grüße,
Dr. med. Joshua Torrent D.
Zitat von Martin Kneppeck am 19. Dezember 2025, 17:01 UhrIm Juni ist ein neuroprotektives Implantat in den USA zugelassen worden, welches die Progression von Mac Tel 2 verlangsamen soll:
Im Juni ist ein neuroprotektives Implantat in den USA zugelassen worden, welches die Progression von Mac Tel 2 verlangsamen soll: